再生醫療產品審查加速 台廠「掛號」申請輔導 食藥署長姜至剛:台灣要走在世界前面
 2026-04-08 10:41
2026-04-08 10:41
- 小
- 中
- 大

圖、文 /財訊雙週刊衛福部積極推動本土再生醫療產品,力拚今年邁入上市階段。負責審查把關的食藥署署長姜至剛親自說明,目前整體進度與政府的監管機制。
圖、文 /財訊雙週刊
衛福部積極推動本土再生醫療產品,力拚今年邁入上市階段。負責審查把關的食藥署署長姜至剛親自說明,目前整體進度與政府的監管機制。
根據《財訊》雙週刊報導,衛福部部長石崇良今年2月公開表示,希望今年能推動再生醫療產品走到上市之路。本土業者雖然信心大振,卻因台廠無取證先例,仍不清楚如何敲開申請大門,投資界也不敢輕舉妄動。3月4日,衛福部食藥署發布「台灣再生醫療製劑輔導專案」,宣示政府將積極輔導;食藥署署長姜至剛透露,已經有一家台廠「掛號」申請輔導了。「我和石部長比業者還緊張!」姜至剛執掌的食藥署,是再生醫療產品能否取證上市的審核單位,面對外界憂心政策會不會只聞樓梯響,不見人下來?姜至剛先展現衛福部的積極態度。
政策催化 再生醫療迎轉折
為什麼再生醫療受到關注與期待?10年前,台灣再生醫療產業才剛萌芽,在衛福部醫事司任職的石崇良積極到日本取經;2018年台灣的細胞治療《特管辦法》上路,產業熱了起來,但《特管辦法》屬於醫院端的醫療技術執行,雖有助累積經驗,卻與真正的取證上市(藥品化)是兩碼子事。由於再生醫療是新興療法,若沒有相對應的法規,廠商會無所適從,食藥署也不敢審;影響所及,沒有藥證就沒有量產,也沒有商業模式,產業根本走不下去。所幸2026年上路的《再生醫療製劑條例》,其中有一項「附款許可」,讓廠商有機會在尚未完成正統三期臨床前,先拿到最多5年的有條件許可,被視為台灣再生醫療商業化的重要轉折。更重要的是,台灣是亞洲繼日本之後,第二個建立完整再生醫療專法的國家,各界都賦予高度期待。站在審核第一線,姜至剛接受《財訊》專訪,回應外界最關切的話題:食藥署如何協助再生醫療廠商走向商業化進程?
姜至剛表示,食藥署在2月4日曾發布《再生醫療製劑查驗登記有附款許可申請須知》,作為初步的申請引導;繼而在3月4日發布「台灣再生醫療製劑輔導專案」(以下簡稱「輔導專案」),透過高密度(原則上每兩週召開一次會議)的雙向溝通機制,輔導國內研發中的再生醫療製劑取得具體成果,當然,其中也包括有附款許可的藥證輔導。「目的就是加速!」姜至剛說。不過,食藥署過去給外界的觀感,都是只敢核准已經拿到美國食品藥物管理局(FDA)等國外藥證的產品;如今面對的是新興療法,全球歷年核可不過百件上下,其中技術先進的產品都是最近十年內的事,有自信走在世界核准之先嗎?姜至剛妙回:「食藥署不是木頭,我們是變形金剛,是有學習能力的。」
審查升級 台廠可望搶先機
他表示,這個輔導專案的團隊,由食藥署主導,包含藥品組與監管組,以及財團法人醫藥品查驗中心(CDE)的專業人員共同組成;也會視需求邀請食藥署的再生醫療諮議小組委員參與,涵蓋學術團體與醫療團體。「這部分不用太擔心,我們比大家還要積極面對這件事。」「石部長與食藥署的想法,是希望在某些領域的核准,走在全世界前面。」姜至剛表示,再生醫療領域很廣,歐美與亞洲關注的方向不太一樣,歐美側重基因治療、基因修飾的細胞治療等;亞洲則比較偏向細胞治療與其衍生物(如外
泌體)。「從製劑端看台灣的再生醫療,非常跟得上腳步。」言下之意,若有符合條件的廠商,食藥署有膽識領先世界核准上市。「我們已經吸收其他國家審查機制的精華,我向同仁說,不用怕!你就去審。我們後面還有很嚴謹的新藥風險管理計畫,監督的網子還能接起來。」姜至剛嚴肅地說,食藥署會特別強化風險管理計畫的監管,重要性等同於前面的審查。
目前,已經有一家廠商「掛件申請」,接下來,輔導專案的團隊會針對業者提供的資訊進行評估,決定是否納入輔導。姜至剛坦言,若是今年內能有公司取證,上半年勢必要有廠商進入專案輔導。根據輔導專案的內容,一旦取得完成輔導證明文件後、提出查驗登記申請,審查天數原則上只需要120天,較一般新藥審查300天縮短不少。
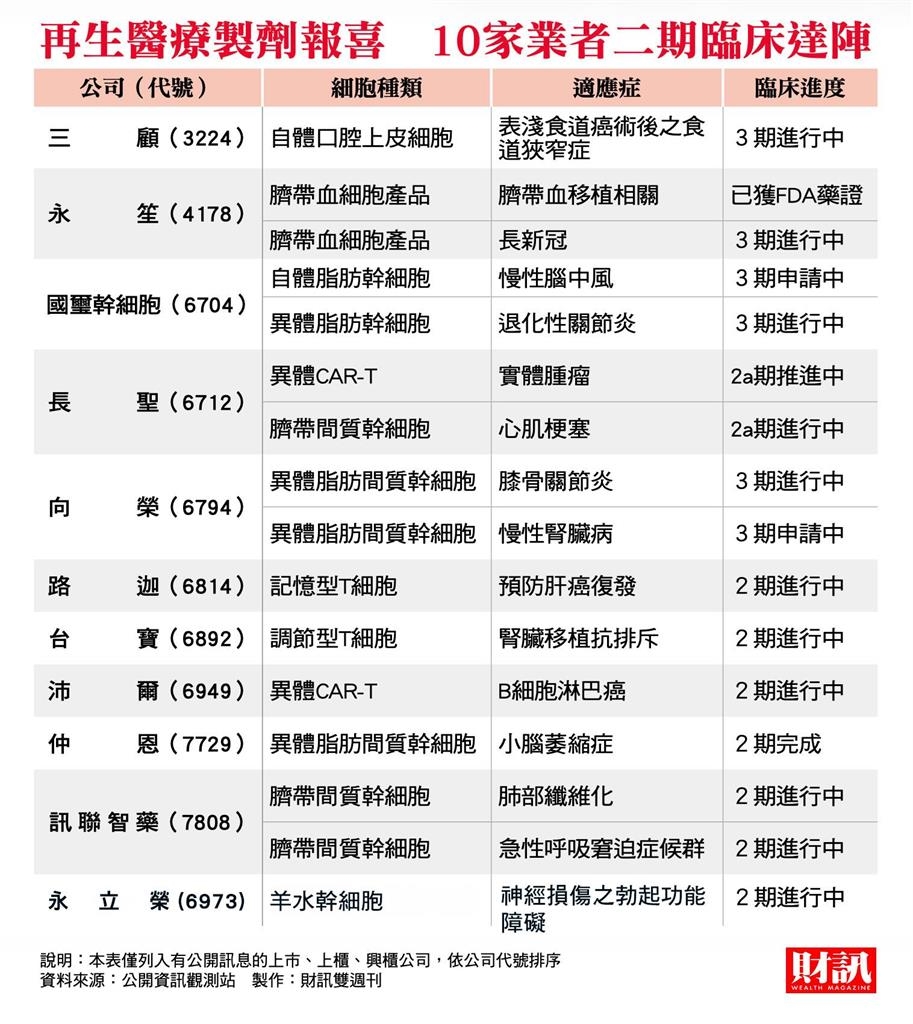
挑戰加大 聚焦適應症界線
據《財訊》了解,由於台廠目前皆尚未完成三期臨床結案,無法申請正常的藥證,想提早上市,須走有條件許可的路徑,也就是該製劑必須完成第二期臨床試驗、且具備安全性及初步療效。目前已有產品達臨床二期的國內業者,大概十多家,誰能納入輔導專案,就相對有機會拿到有條件許可。對於再生醫療而言,安全性、療效,以及製程品質是最基本的前提,本來就有非常嚴謹的審核標準,反倒是想要提前拿到有條件許可的另一個條件——適應症必須涉及「危及生命或嚴重失能疾病」。套一句姜至的說法,「這是一個大哉問!」舉例來說,若是超高齡長者,讓他做膝關節手術可能風險很高,但不做可能失能,如果有再生醫療可以達到效果,這算不算符合危及生命或嚴重失能疾病?「現在大家會擔心就是這件事;到底該是多寬多鬆?假如很浮濫,對於再生醫療是一種傷害」。姜至剛表示,現在雖然無法有正確答案,但是食藥署會邊走邊看。「一開始畫的線不能太窄,否則所有的適應症都沒有空間;覺得有需要,再調整收窄。」他強調,在考量適應症是否能納入輔導專案時,也會做很多風險、效益、經濟面的共同考量,「不是單純有效沒效,還要附加在原來的治療基礎上,否則民眾會被誤導。」
《財訊》採訪得知,今年2月,日本傾國家之力發展逾十年的誘導性多功能幹細胞(iPS細胞),終於以附條件、附期限的方式,領先全世界核發重度心衰竭與帕金森氏症的兩張細胞治療藥證,給了台廠激勵與壓力。
3月中旬,台灣醫界聯盟基金會執行長林世嘉,組隊6家生技公司赴日本再生醫學會年會參展,她表示,台灣再生醫療產業正邁入制度化與產業化的新階段,我們的制度設計與日本相近,雙方具有高度互補性。姜至剛也說,再生醫療產業發展離不開國際合作,因此食藥署也會與其他國家協商「信賴審查」,將雙方互相核准的門檻調整到比較一致;目前日本是主要的商談對象。
…(更多精彩內容,詳見《財訊》雙週刊第760期)
延伸閱讀:
面板展不再只秀面板!2026 Touch Taiwan聚焦矽光子與先進封裝
房市有回暖跡象?建商預估:央行逐步放寬管制帶動成交比率 全年移轉棟數將維持
26萬至28萬棟水準
即使荷姆茲海峽仍封鎖,川普也願意結束伊朗戰爭?市場從3個角度解讀可能發展
延伸閱讀

從7歲就開始助選 力拚台南第一女市長 陳亭妃 用勤跑基層打造選民感情黏著度
2026-04-08 10:41

舔不得!人氣冰淇淋「ICC」出包 進口紙托檢出螢光增白劑
2026-04-07 10:59

房市有回暖跡象?建商預估:央行逐步放寬管制帶動成交比率
2026-04-08 10:41
 {PLAYICON}
{PLAYICON}面板展不再只秀面板!2026 Touch Taiwan聚焦矽光子與先進封裝
2026/04/08 10:41:27
 {PLAYICON}
{PLAYICON}美伊停火台股狂飆1213點 台積電上漲80元衝到1940元
2026/04/08 10:14:12
 {PLAYICON}
{PLAYICON}睫毛上其實有蟲!醫曝「九成人中招」:嚴重恐掉睫毛…6症狀要注意
2026/04/08 09:45:43

